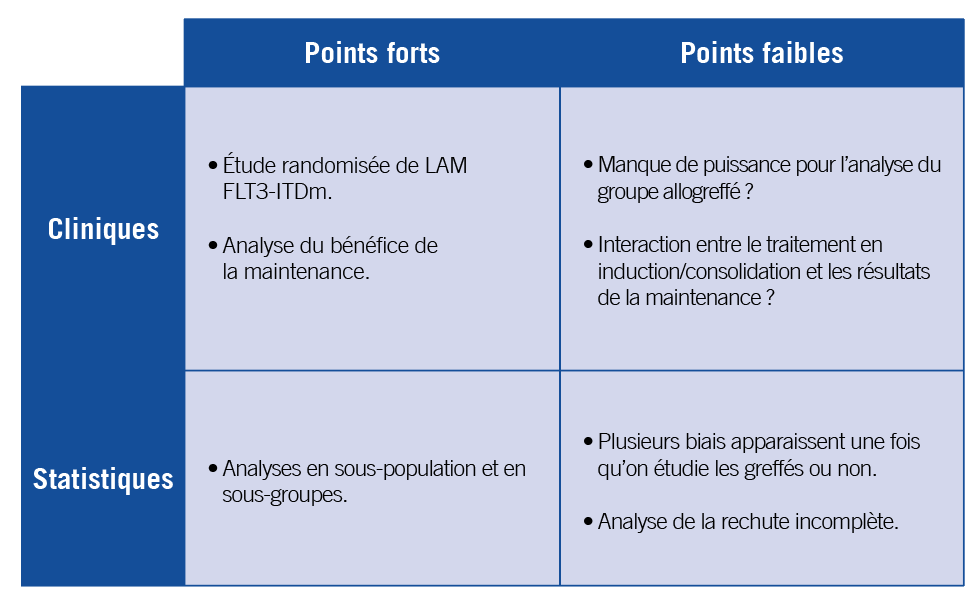
À quoi sert la maintenance par quizartinib pour les LAM FLT3+ ?
QUANTUM-FIRST : efficacité du traitement de maintenance chez les patients nouvellement diagnostiqués d’une LAM avec mutation de FLT3-ITD.
QUANTUM-FIRST: efficacy in newly diagnosed patients with fms-like tyrosine kinase 3-internal tandem duplication–positive (FLT3-itd+) acute myeloid leukemia (AML) who received continuation therapy.
D’après la communication orale de Sekeres MA et al. Abstract #S142, EHA 2024.
Contexte de l’étude
La prise en charge des LAM FLT3 ITD mutées repose actuellement sur la chimiothérapie intensive avec un inhibiteur de FLT3 (midostaurine). La question de la maintenance chez les patients allogreffés ou non reste débattue. Le quizartinib (Quiz) a démontré son efficacité en matière avec l’amélioration de la survie globale avec les résultats de l’étude QUANTUM-FIRST (Erba et al., Lancet 2023). Le Quiz est maintenant autorisé en induction consolidation et entretien aux États-Unis et en Europe après avoir démontré une réduction du risque de décès de 22 % par rapport au placebo. Il n’a en revanche pas d’autorisation de maintenance après allogreffe.
Objectifs de l’étude
L’objectif de cette étude est d’évaluer l’impact du traitement d’entretien sur l’efficacité du Quiz chez les patients atteints de LAM FLT3-ITDm traités dans l’étude QUANTUM-FIRST, avec une analyse sur la survie, la survie sans rechute et l’incidence cumulée de rechute chez les patients poursuivant le Quiz.
Résultats de l’étude
L’étude Quantum-First a inclus 539 patients de 18-75 ans avec une LAM FLT3-ITDm nouvellement diagnostiquée. Les patients ont été randomisés (1:1) dans un bras placebo (n=271) ou Quiz (n=268) en plus d’un traitement d’induction (2 cycles 3+7), de consolidation (4 cycles HiDAC) et d’une phase de maintenance allant jusqu’à 36 cycles. Cent seize patients ont reçu le traitement par Quiz et 92 le placebo en maintenance. Dans le plan statistique, il était prévu une analyse de la survie et de la survie sans rechute chez les patients recevant une maintenance. La médiane d’âge était de 53 ans dans le groupe Quiz et de 56 ans dans le groupe Placebo. Le groupe Quiz et Placebo avaient respectivement 59 % et 65 % de mutation NPM1, une ECOG-PS à 2 de 14.7 % et 7.6 %, une leucocytose >40 G/L chez 50.9 % et 37 % des patients. L’analyse de la survie globale montre un bénéfice non significatif à 24 mois (87.8 % vs 78.1 %), 36 mois (79.9 % vs 71.1%), et 48 mois (76.3 % vs 67.9 %) avec un HR de 0.683 (0.395-1.183, figure 1).
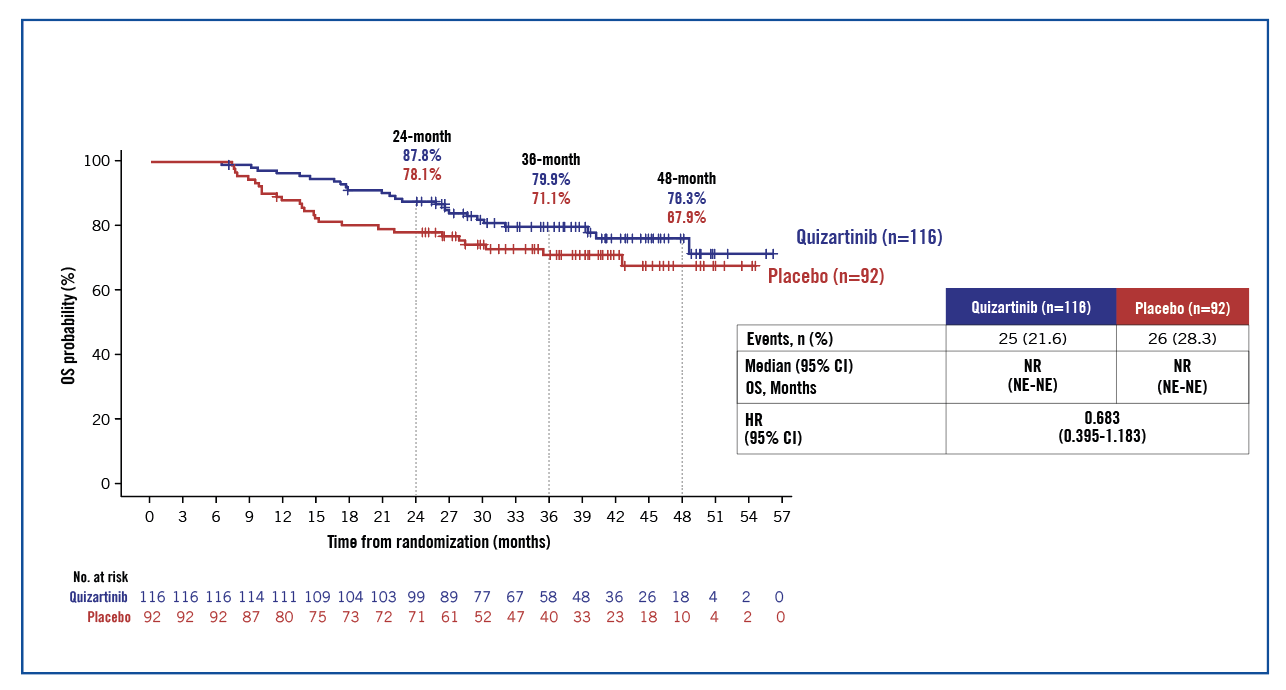
Figure 1 : survie globale.
L’analyse de la survie sans rechute (figure 2) ne montre pas de bénéfice significatif malgré des taux d’EFS à 12 mois de 92.4 % vs 80.6 %, à 24 mois de 73.2 % vs 64.9 %, à 36 mois de 67.1 % vs 59.6 % (HR=0.738 ; 0.442-1.23). L’incidence cumulée de rechute à 12, 24 et 36 mois est de 6.5 % vs 16.7 %, 22.3 % vs 30.9 % et 25.9 % vs 34.4 %. L’analyse de la survie et de la survie sans rechute à l’aide d’un score de propension avec ajustement sur les variables de baseline (âge, sexe, NPM1, leucocytose, pourcentage de blastes), l’allogreffe et le type d’anthracycline, ne montre aucun bénéfice significatif en faveur du bras quizartinib.
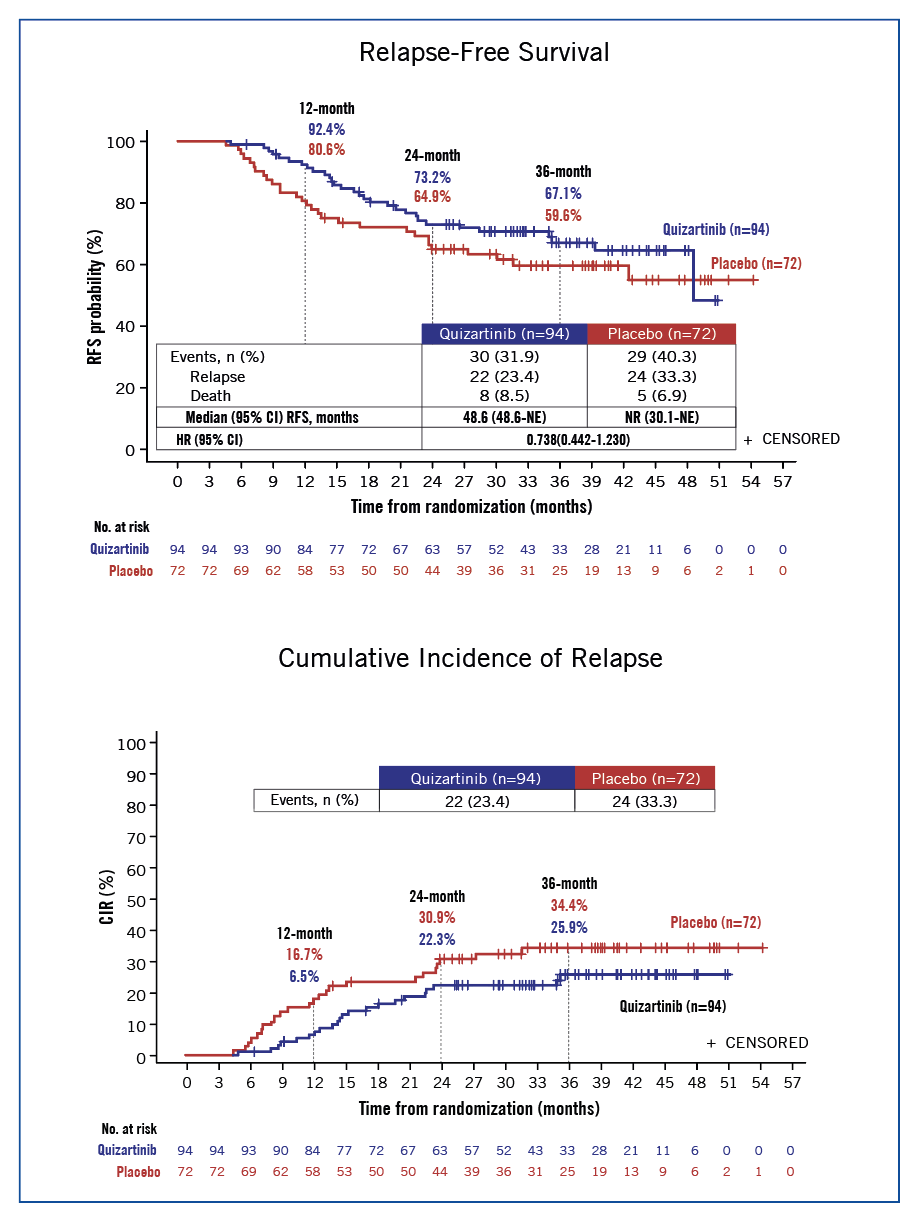
Figure 2 : survie sans rechute et incidence cumulée de rechute selon le traitement d’entretien par quizartinib ou placebo.
Parmi les patients qui ont reçu une allogreffe de consolidation, 71 % des patients du bras Quiz et 55 % du bras Placebo ont pu recevoir la maintenance, et la différence est principalement due à des rechutes post-allogreffe ou une absence de critère permettant de mettre en place le traitement de maintenance (cytopénies ?).
La courbe de survie des patients allogreffés selon le traitement reçu en maintenance ne montre pas de différence avec une médiane de suivi de 39.2 mois (HR=1.622 ; 0.623-4.220). Les auteurs pointent la possible responsabilité d’un nombre limité d’évènements (20) et un plus faible nombre de patients ayant reçu la maintenance dans le bras placebo pour expliquer l’absence de différence probante.
En revanche, dans le groupe non-allogreffé en consolidation, un bénéfice de survie en faveur du bras Quiz est trouvé :
HR=0.401 (0.192-0.838) soit une réduction du nombre de décès de 60 %.
Concernant la tolérance, il a été observé davantage d’évènements de grade 3 ou plus liés au traitement par le Quiz (53 % vs 17 %) avec notamment une interruption de dose chez 39.7 % des patients dans le bras Quiz (12 % bras PBO) et une diminution de dose chez 27.6 % (contre 8.7 % bras PBO). Les évènements sont des neutropénies de grade 3 ou plus (31 % vs 4 %), surtout bien qu’il y ait eu également davantage de diarrhée, de nausées, mais de grade <3 pour la plupart.
Quels impacts sur les connaissances et les pratiques cliniques ?
Cette étude démontre l’intérêt du quizartinib en traitement de maintenance dans une population de LAM FLT3-ITDm ne recevant pas d’allogreffe. Après allogreffe, le bénéfice reste incertain et ne permet pas de traiter les patients dans cette indication. Il sera sans doute utile d’avoir les analyses de maladie résiduelle qui permettront de sélectionner (peut-être) au mieux les patients bénéficiant du traitement de maintenance par quizartinib.
Le quizartinib rejoint la midostaurine au rang des traitements des patients atteints de LAM FLT3-ITD mutée.
La tolérance du traitement en maintenance semble acceptable même s’il y a eu de nombreuses réductions et interruptions de traitement.
Critique méthodologique
Les analyses qui ont été présentées font suite à l’essai clinique comparant le quizartinib (Quiz) versus placebo dans une cohorte de patients LAM positifs à la mutation FLT3. Le but ici est d’afficher les résultats exploratoires obtenus sur une sous-population de patients ayant bénéficié d’un traitement de maintenance, sur deux endpoints principaux (voir Focus statistique) que sont la survie globale (OS) et la survie sans rechute (RFS).
Sur 288 patients inclus dans le bras quizartinib, 173 ont été jusqu’à la consolidation et 116 ont été éligibles au traitement de maintenance, tandis que dans le bras placebo, 271 ont été inclus, 175 ont reçu ce traitement en consolidation et 92 ont pu l’obtenir en traitement de maintenance. À noter que le traitement de maintenance a été effectué avant ou après la greffe. Car il est toujours à craindre dans ce type d’étude exploratoire post-essai clinique que le profil de patients suivis évolue au cours du temps. Par conséquent, les deux sous-populations de patients ayant reçu un traitement de maintenance affichent des différences de caractéristiques entre ceux issus du groupe Quiz et ceux du groupe Placebo.
Voici une liste non-exhaustive de différences statistiques observées :
– les patients du bras Quiz sont plus jeunes d’environ 3 ans ;
– quasiment 15 % de scores ECOG 2 dans ce sous-groupe et deux fois moins pour le bras placebo ;
– une fréquence moindre de mutations NPM1 chez les Quiz ;
– une proportion de patients ayant un VAF de FLT3 + < 25 % plus importante, toujours chez les
Quiz ;
– et enfin, plus d’allogreffes effectuées (70 contre 49 chez les malades issus du bras Placebo).
Autant de facteurs de confusion à considérer.
En univarié, les deux sous-populations affichent une survie équivalente avec un hazard-ratio (HR) de 0.683 [0.395-1.183], donc non-significatif. Pareillement pour la RFS avec un HR égal à 0.74 [0.44-1.25], la p-value est logiquement non-significative au seuil de 5 %. Les auteurs ont bel et bien effectué un ajustement en tenant compte des facteurs de confusion (dont la greffe) en effectuant un appariement par score de propension, et là de nouveau, la comparaison entre placebo et Quiz ressortait non-significative. Une analyse d’incidence de rechute a été effectuée mais sans calculer de HR de sous-distribution, ni effectuer de comparaison statistique, encore moins d’analyse multivariée ajustée. On sait simplement que l’incidence de rechute au dernier follow-up est de 23.4 % pour la sous-population Quiz contre 33.3 % pour placebo, sans plus de détails. Cela méritait pourtant d’être approfondi.
En réalisant des analyses de sous-groupes parmi les allogreffés, on ne constate aucune différence de survie également alors que c’est le cas chez les non-greffés : HR=0.40 [0.19-0.83] en faveur du bras quizartinib.
Attention : on ne connait pas le descriptif comparatif Quiz vs placebo de la population greffée. Autre biais : on étudie des patients éligibles à la greffe, il y a donc un biais de sélection.
Ce résultat qui ressort positif malgré les biais observés restera-t-il dans une impasse ?