Une séance plénière accordée à la LMC !
Optimiser la balance bénéfice/risque avec en ligne de mire la TFR
C’est peut-être abandonner les ITKs de 1re et 2e génération en première ligne ?
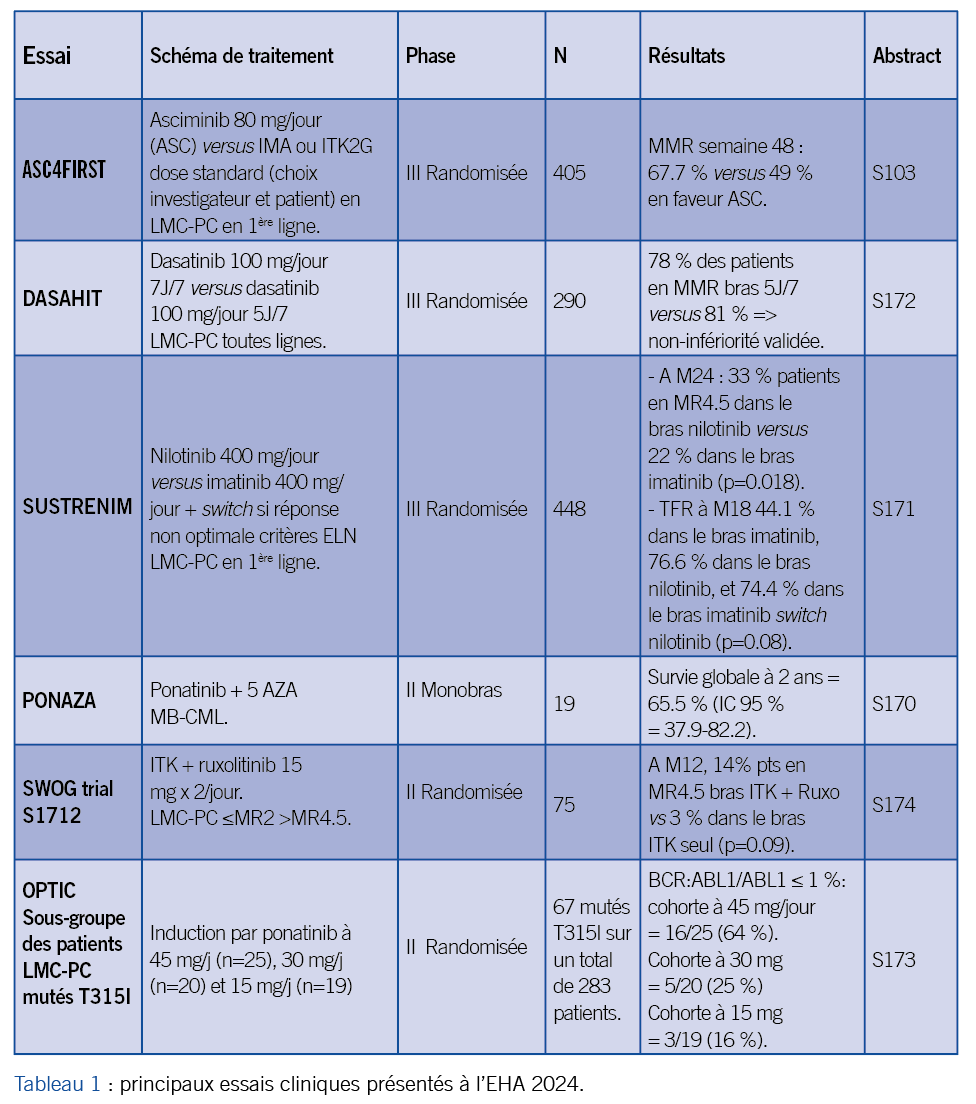
Les résultats de l’étude ASC4FIRST testant l’asciminib (ASC) en première ligne versus les inhibiteurs de tyrosine kinase (ITK), imatinib ou ITK2G, choisis par l’investigateur et le patient, ont en effet été présentés en session plénière. Les standards de prise en charge des patients sont bousculés dans la LMC ! Les résultats obtenus en termes de rémission moléculaire majeure (MMR pour major molecular remission) à 1 an ont été communiqués ; pour les données d’éligibilité à l’arrêt de traitement et de TFR il va falloir encore attendre !
En attendant quoi de neuf côté ITK2G ?
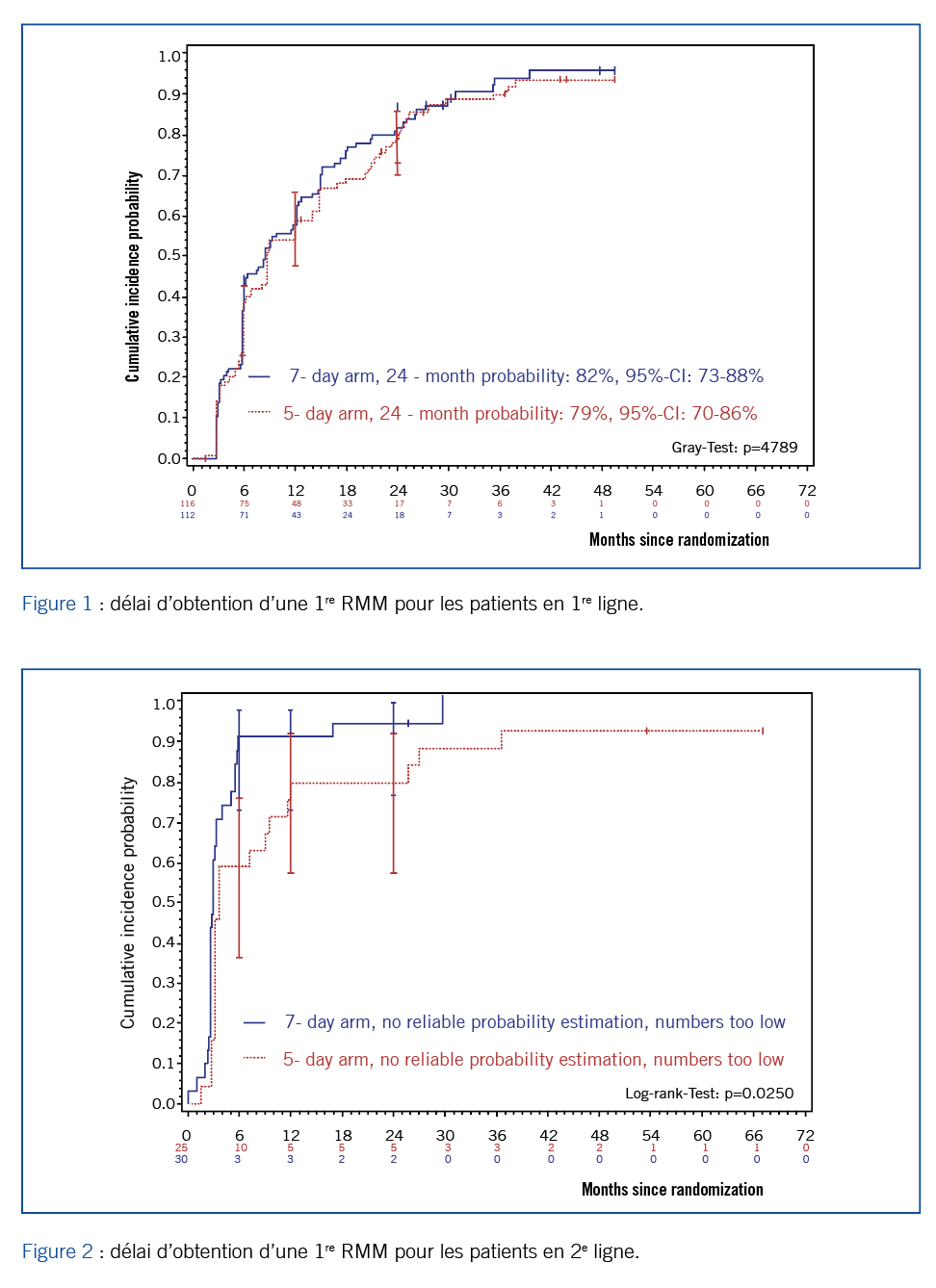
Paul LaRosée a présenté en communication orale les résultats finaux de l’étude allemande DASAHIT (Dasatinib Holiday For Improved Tolerability) réalisée entre août 2016 et mars 2021 (#S172). Il s’agit d’un essai de phase III, prospectif, randomisé de désescalade de la dose, testant la non-infériorité d’un schéma d’administration du dasatinib 100 mg/jour, 5 jours sur 7 (bras expérimental) versus une administration quotidienne à 100 mg/jour (bras contrôle), sur le critère taux de MMR à M24. Le rationnel de l’étude repose sur les propriétés pharmacocinétiques du médicament. L’objectif secondaire était de diminuer la toxicité du médicament, en particulier l’incidence des épanchements pleuraux. Sur les 290 patients randomisés, 80 % étaient en 1ère ligne et 20 % résistants ou intolérants en 2e ligne et au-delà. À 24 mois, l’hypothèse de non-infériorité a été validée avec 78 % des patients en MMR dans le bras expérimental versus 81 %. Cependant s’il n’y a pas de différence en termes d’incidence cumulée de MMR entre les 2 bras concernant les patients en 1re ligne (figure 1), ce n’est pas le cas pour les autres patients (figure 2). On retiendra également de cette étude une réduction de 50 % de l’incidence des épanchements pleuraux dans le bras expérimental !
Massimo Breccia nous a offert une actualisation de l’essai SUSTRENIM avec notamment des données de TFR à 18 mois chez des patients suivis dès le diagnostic et traités soit par nilotinib 600 mg/jour soit par imatinib 400 mg/jour avec switch pour nilotinib en cas de réponse non optimale selon les critères ELN 2013.
LMC et situations péjoratives
Philippe Rousselot a présenté en communication orale les résultats de l’essai PONAZA concernant les patients LMC en transformation blastique myéloïde (MB-CML).
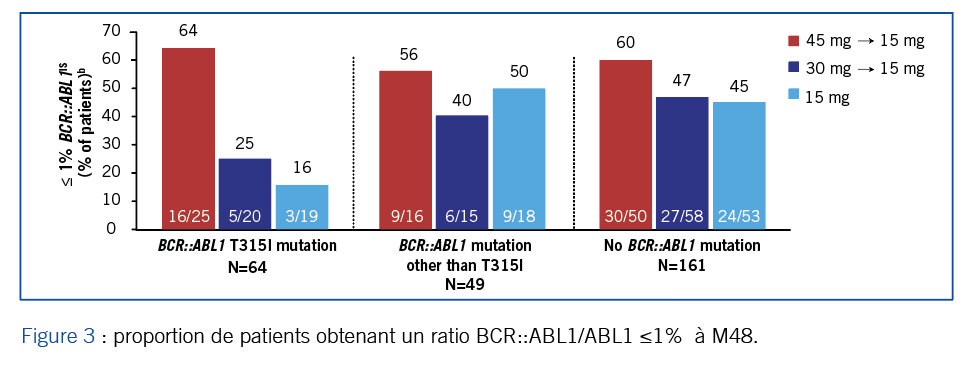
Jane Apperley a exposé des données actualisées à 4 ans (cut off 08/05/23) concernant les patients mutés T315I inclus dans l’étude OPTIC. Pour rappel cet essai de phase II s’adressait à des patients LMC en phase chronique (PC) résistants à ≥ 2 ITK ou mutés T315I qui ont été randomisés pour recevoir 3 dosages différents de ponatinib en induction : 45 mg/jour (n=94), 30 mg/j (n=95) ou 15 mg/j (n=94). Une désescalade à 15 mg par jour était pratiquée pour les patients initiés à 45 et à 30 mg par jour dès l’obtention d’un ratio BCR::ABL1/ABL1 ≤ 1 %. La proportion de patients T315I mutés est de 27 % dans la cohorte 45 mg/jour et de 22 % dans les 2 autres cohortes. L’efficience de l’induction à 45 mg/jour par rapport aux autres dosages (30 mg et 15 mg) est la plus marquée au sein des patients T315I mutés comparativement aux sous-groupes de patients non mutés ou autres mutations aussi bien sur la proportion de patients obtenant un ratio BCR::ABL1/ABL1 ≤ 1 % (critère de jugement principal) (figure 3) ou une réponse de type MR4.5. Concernant les patients T315I mutés, la médiane de survie sans progression n’est pas atteinte dans le bras 45 mg/j, alors qu’elle est de 28.4 mois et 45.6 mois dans les cohortes
30 mg/j et 15 mg/j respectivement. La médiane de survie globale n’est atteinte dans aucune des 3 cohortes. Soulignons l’efficacité de la réescalade de dose en cas de perte de réponse après réduction de dose. D’un point de vue tolérance, on note 52 % versus 29 % d’évènements indésirables de grade 3-4 dans le bras 45 mg versus 15 mg, et un taux faible d’évènement occlusif artériel émergent sous traitement.
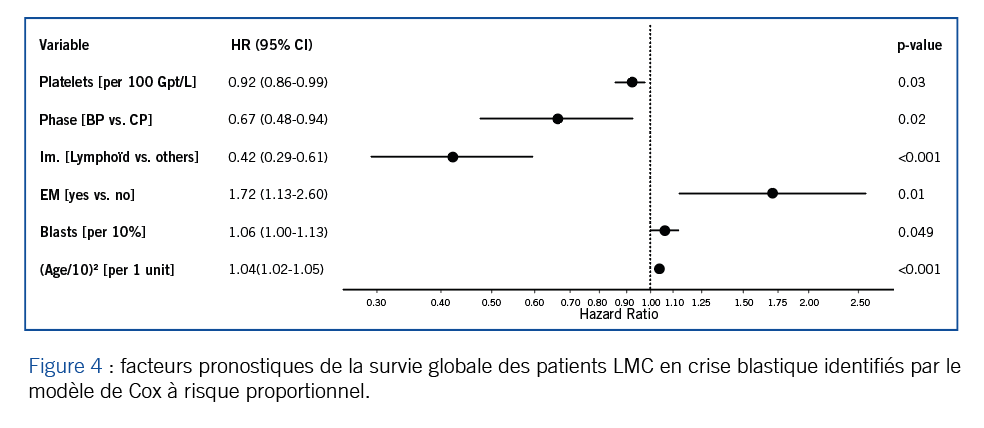
Lauseker M et al ont quant à eux présenté un abstract sur l’établissement d’un score pronostique pour les patients LMC en phase blastique (CML-BP), ce dernier a été établi à partir du registre européen « European Leukemia Net Blast Phase Registry ». Avec un délai médian d’observation de 45 mois (à partir du diagnostic de BP), la survie médiane des 275 patients inclus est de 18.9 mois [IC de 95 % 16.8-26.1 mois]. Ils ont identifié 6 facteurs pronostiques clés de la survie globale (OS pour overall survival) grâce à un modèle de Cox à risque proportionnel :
le pourcentage de blastes dans le sang périphérique, la numération des plaquettes, l’âge au diagnostic de BP, la phase au diagnostic de la LMC (BP vs CP), l’immunophénotype (lymphoïde vs autres) et la présence d’une maladie extramédullaire (figure 4). Sur cette base, le score développé classe : 14 % des patients en risque faible avec une OS médiane de 97 mois [67 mois -non atteint], 59 % en risque intermédiaire avec une OS médiane de 22 mois [18-35] et 27 % en risque élevé avec une OS médiane de 9 mois [6-13].